Резюме
- Исследователи лечили серповидно-клеточную анемию у мышей, напрямую редактируя дефектный ген гемоглобина, вызывающий это заболевание.
- Эти результаты могут привести к одноразовому лечению серповидно-клеточной анемии с меньшим количеством побочных эффектов, чем другие методы лечения, находящиеся в разработке.
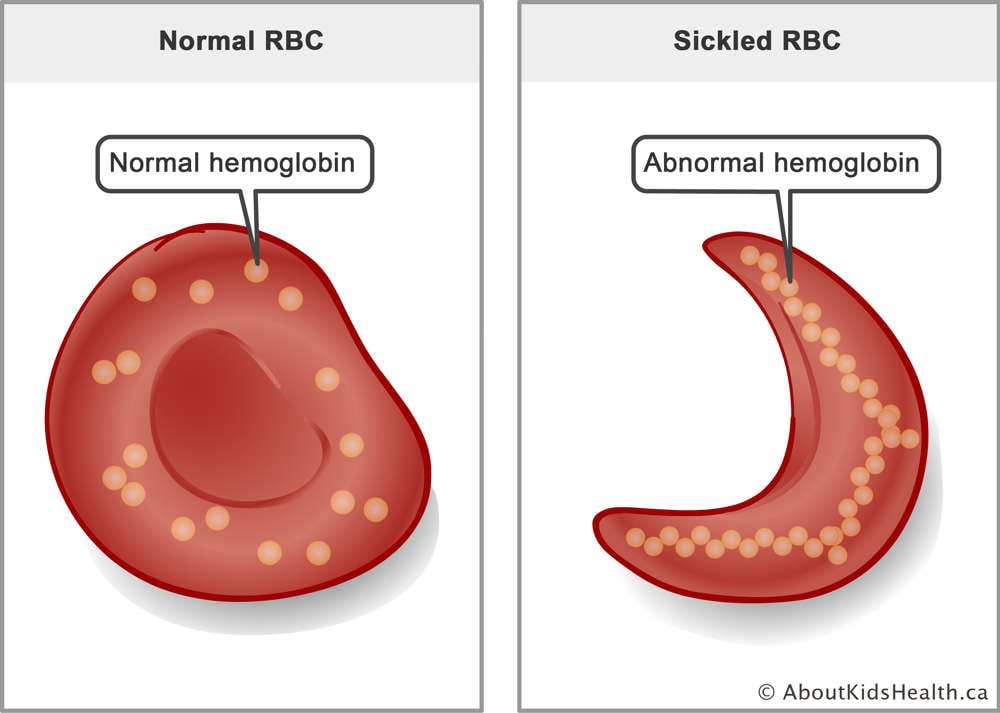
Серповидно-клеточная анемия (SCD) – это генетическое заболевание, вызванное мутацией в обеих копиях человеческого гена HBB. Этот ген кодирует компонент гемоглобина, который является белком, переносящим кислород в красных кровяных тельцах. Мутация заставляет молекулы гемоглобина слипаться, создавая серповидные эритроциты. Этот процесс может привести к разрыву клеток крови, анемии, повторяющейся боли, иммунодефициту, повреждению органов и ранней смерти. Трансплантация костного мозга может вылечить ВСС, но подходящего донора найти трудно. Процедура трансплантации также сопряжена с риском возникновения опасных побочных эффектов.
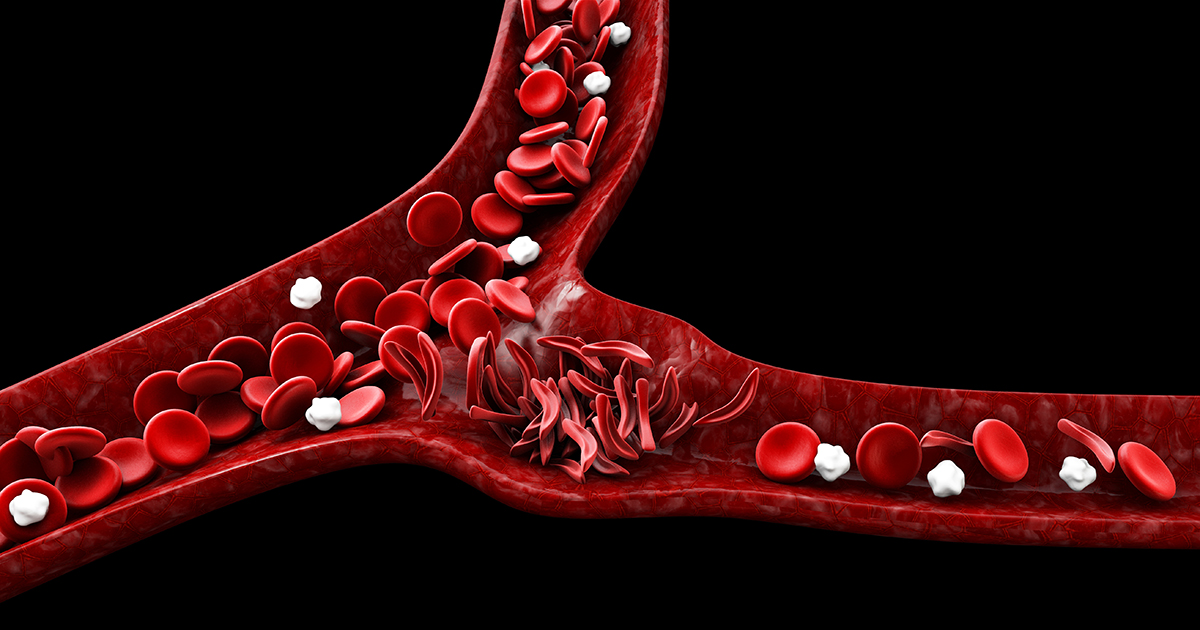
В настоящее время разрабатываются несколько новых методов лечения серповидно-клеточной анемии. Эти методы включают редактирование генов собственных клеток костного мозга пациента для производства нормально функционирующего гемоглобина. Эти методы лечения позволяют избежать рисков, связанных с трансплантацией костного мозга. Но эти методы также несут в себе риски, потому что они включают введение новой ДНК и расщепление существующих цепей ДНК.
Группа исследователей во главе с доктором Дэвидом Лю из Института Броуда и доктором Митчеллом Вайсом и доктором Джонатаном Йеном из детской больницы Св. Джуда в США разработала метод, позволяющий избежать некоторых рисков, связанных с другими подходами к редактированию генов. В этом методе используется молекулярный метод, называемый базовым редактированием, при котором изменяется одна буква генома без разрезания ДНК.
При серповидно-клеточной анемии Т заменяет А в ключевом месте гена HBB. Хотя базовое редактирование не может отменить это изменение, вместо этого оно может преобразовать T в C. Это действие производит естественный, непатогенный вариант гемоглобина, называемый Hb-Makassar. Исследователи разработали молекулярный инструмент, называемый редактором оснований аденина, который распознает мутировавшую часть гена и преобразует T в C.
Исследователи использовали редактор баз аденина на кроветворных стволовых клетках пациентов с ВСС. До 80% клеток имели ген серповидноклеточного гемоглобина, преобразованный в вариант Макассара. Для тестирования команда трансплантировала отредактированные человеческие клетки в мышиную модель SCD. Через 16 недель после трансплантации 68% донорских стволовых клеток имели гены HBB, отредактированные до Hb-Makassar. Эритроциты, полученные из этих стволовых клеток, значительно уменьшили серповидность.
Поскольку человеческие эритроциты не могут выжить у мышей достаточно долго для всестороннего тестирования, команда затем взяла стволовые клетки из мышиной модели SCD, отредактировала их и трансплантировала отредактированные клетки другой группе мышей. Через 16 недель вариант Макассара составлял почти 80% гемоглобина у мышей-реципиентов. Контрольные мыши, получившие неотредактированные клетки, имели характерные симптомы ВСС: анемия, аномальное количество клеток крови, серповидные эритроциты и увеличенная селезенка. У мышей, которым вводили отредактированные стволовые клетки, симптомы значительно улучшились.
Исследователи взяли костный мозг у мышей, получивших отредактированные стволовые клетки, и трансплантировали его новой группе мышей. У новых реципиентов был здоровый подсчет кровяных телец, подтверждающий надежность редактирования генов. Исследователи также определили, что редактирования не менее 20% копий гена SCD было достаточно для поддержания здоровых показателей крови. Они не обнаружили никаких побочных эффектов у мышей от процесса редактирования генов.
«Этот подход предлагает многообещающую основу для одноразового или, возможно, даже одноразового лечения серповидно-клеточной анемии», – говорит Лю.
В настоящее время команда работает над дальнейшим развитием концепции с конечной целью – охватить пациентов.
.









:max_bytes(150000):strip_icc()/GettyImages-86013044-5ba93f1a46e0fb00258771d9.jpg)
Discussion about this post